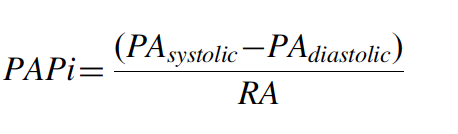Cuidados ao se indicar um dispositivo
Quando indica-se um dispositivo de assistência circulatória esquerda, deve-se tomar alguns cuidados para:
1) Indicar o dispositivo certo para o paciente
2) Minimizar complicações após o implante
3) Avaliar contra-indicações
A) Avalie o Ventrículo Direito
Após o implante do dispositivo de assistência circulatória espera-se que aumente-se o débito cardíaco do paciente, como o Ventrículo Esquerdo e o Ventrículo direito trabalham em um circuito fechado, o débito das duas câmaras é o mesmo, e antes do implante do dispositivo de assistência circulatória ao ventrículo esquerdo ( LVAD – Left Ventricle Assist Device) deve-se verificar se o paciente não apresenta alto risco de disfunção de ventrículo direito após o implante do dispositivo . Não há definição na literatura sobre quais parâmetros utilizar mas em geral baseia-se em:
I) Ecocardiográficos: disfunção de VD, diâmetro do VD aumentado, TAPSE < 7,5, Insuficiência tricúspide importante associada com disfunção de VD
II) Hemodinâmicos: PAD>15, relação PVC/PCP > 0,63, RVP > 8 Woods, GTP > 12, GDP > 5
III) Clínicos-laboratoriais: disfunção hepática, congestão direita franca, disfunção renal importante
Nestes casos em que tudo indica que o VD não suportará a “ajuda” ao VE, se permanecer a indicação clínica de suporte circulatório deve-se indicar um suporte Biventricular. Cabe ressaltar que a indicação de suporte biventricular ao invés de suporte univentricular esquerdo não baseia-se apenas em algum dos fatores acima mas no conjunto dos fatores e individualizos para a situação clínica de cada paciente. Talvez no futuro defina-se uma maneira mais objetiva de se determinar – através de um score – quem deve ou não receber o dispositivo biventricular. Em artigos recentes um parâmetro que tem predito com alto grau de acurácia aqueles pacientes que irão evoluir com disfunção de VD – mas ainda não testado prospectivamente – é o índice de pulsatilidade da artéria pulmonar, definido como PAS – PAD da artéria pulmonar / Pressão no átrio direito. Pacientes com índice > 2,0 em geral não evoluem com disfunção de VD após implante do LVAD ( Left Ventricule Assist Device) e índices menores que 2,0 tem grandes chances de evoluirem com disfunção de VD ( Sensibilidade de 74% e Especificidade 67% para necessidade de suporte do VD após o implante). Éimportante calcular esse índice antes de se indicar o dispositivo, mas sempre tome a decisão sobre o tipo de dispositivo ( uni ou biventricular ) baseado em todas as características do paciente.
Porque Acontece ?
– o VD as vezes não suporta o aumento da pré-carga gerado pelo dispositivo esquerdo ( lembre que o débito do VE = débito do VD)
– o desvio do septo para dentro do VE – secundário ao esvaziamento do VE pelo dispositivo – afeta a interdependência ventricular, diminuindo a capacidade do VD de ejetar sangue ( estima-se que 20% a 40% do débito do VD dependa da contratilidade do ventrículo esquerdo e da interdependência ventricular).
– O desvio do septo também piora a insuficiência tricúspide pela deslocamento anatómico do anel valvar da tricúspide, aumentando o volume de sangue regurgitante e diminuindo o fluxo de sangue pela artéria pulmonar
B) Valvopatias
Avaliar se o paciente não tem valvopatia importante que deve ser corrigida no mesmo tempo cirúrgico principalmente Insuficiência aórtica (em dispositivos VE-Ao se houver Insuficiência Aortica importante forma-se um circuito em alça fechada em que o sangue ejetado pelo dispositivo retorna para o ventrículo esquerdo pela valva aórtica incompetente, sem fluxo anterógrado do sangue). Deve-se corrigir no momento do implante do dispositivo as valvopatias aórticas. Insuficiência tricúspide moderada ou grave também deverá ser corrigida. Para as valvopatias mitrais deve-se corrigir a estenose moderada ou importante, a insuficiência em geral não necessita de intervenção a menos que haja possibilidade de recuperação do VE ( “ponte para recuperação”) nestes casos pode-se corrigir a insuficiência mitral, desde que esta seja moderada ou grave.
C) Anticoagulação
Certifique-se que o paciente tolera a anticoagulação e não apresenta nenhuma contraindicação absoluta ao uso de warfarina uma vez que pacientes com dispositivos de assistência circulatória de médio/longo-prazo deverão ser anticoagulados (para os dispositivos atuais que são de fluxo contínuo – não pulsátil). Para dispositivos de curto-prazo a necessidade de anticoagulação varia de acordo com o dispositivo e não é mandatória. Para os dispositivos de curto-prazo o único em que a anticoagulação não é obrigatória é o Balão Intra-Aórtico.
D) Suporte Social
Um dispositivo de longa permanência requer muitos cuidados e compreensão pela família/paciente dos seus riscos, bem como da mudança no padrão de vida daqueles indivíduos portadores de dispositivos. Os pacientes devem receber aulas sobre o manejo do dispositivo em casa e devem se mostrar hábeis para o manejo do dispositivo.
E) Dispositivo de curta duração x longa duração
Pacientes com choque cardiogênico em INTERMACS 1 apresentam grande mortalidade ( ~50%) quando submetidos ao implante de um dispositivo de longa duração, baseando-se nisso a tendência atual é implantar um dispositivo de curta duração – cuja inserção é mais rápida e fácil, associada com menor riscos intrínsecos ao procedimento – como uma método de ‘ponte para ponte’, isto é, para a inserção posterior de um dispositivo de longo prazo. Em geral pacientes com choque cardiogênico refratário necessitam de uma intervenção rápida (horas) ou o paciente evoluirá para disfunção múltipla de órgãos e morte, por conta dessa ‘pressa’ por muitas vezes não é possível se definir se o paciente é de fato um candidato para suporte circulatório de longo prazo ( status neurológico incerto, suporte social, pagamento pelo convênio, avaliação de contra-indicações para o dispositivo e invariavelmente problemas relacionados ao serviço de saúde: disponibilidade de sala cirúrgica, anestesista, cirurgião cardíaco, etc). Ressalta-se que se pacientes em perfil INTERMACS 1 não é contra-indicado o implante de dispositivo de longa permanência desde que sua elegibilidade esteja bem definida e as contra-indicações excluídas, no registro INTERMACS por exemplo aproximadamente 16% dos dispositivos são implantados em pacientes com este perfil, mas este número vem caindo progressivamente pelas condições descritas acima e pela melhora exponencial de dispositivos de curta duração
 |
|
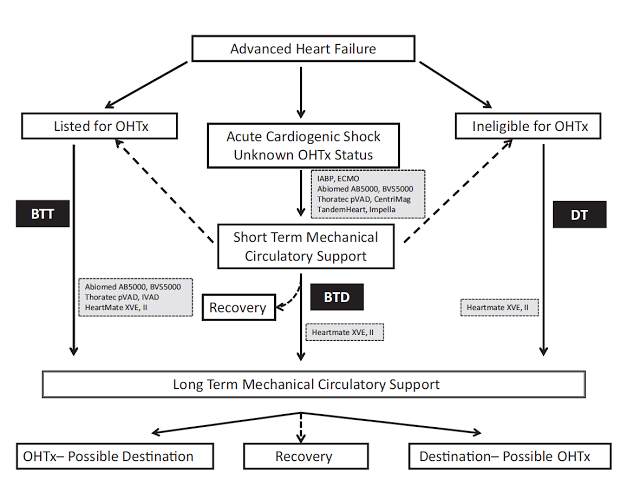
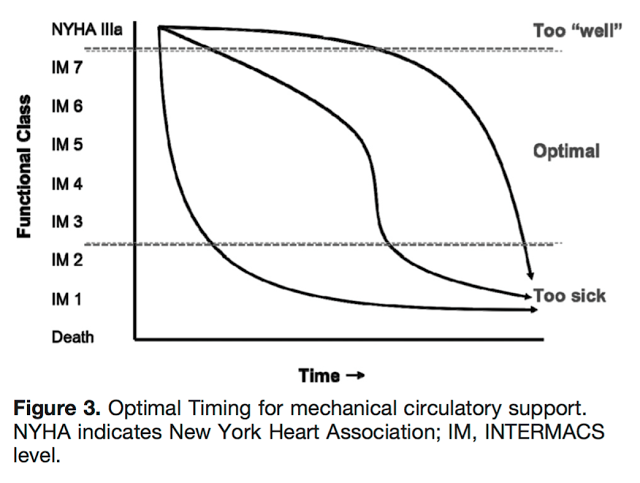
“Timing” ideal para se indicar um dispositivo de assistência circulatória de longo prazo. Fonte: Peura et al. Recommendations for the use of mechanical circulatory support. Circulation 2012
|
F) Contraindicações absolutas para dispositivos de longa permanência:
– insuficiência hepática, renal (IRC dialítica antes da internação) e neurológica irreversíveis
– não-aderência medicamentosa
– limitações sociais muito graves
– comorbidades graves com expectativa de vida menor que 1 ano
 |
|
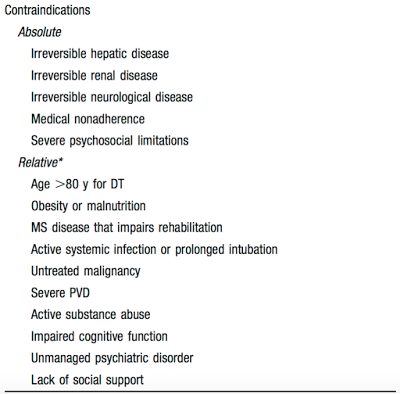
Contraindicações relativas e absolutas de suporte circulatório de longo prazo. Fonte: Peura et al. Recommendations for the use of mechanical circulatory support. Circulation 2012
|
Leitura Recomendada:
1) Peura et al. Recommendations for the use of mechanical circulatory support. Circulation 2012
2) International Society for Heart and Lung Transplantation Guidelines for mechanical circulatory support. JHLT 2013
3) Kang et al. PAPi Predicts RVF After LVAD Implantation. JHLT 2016
4) Eliott et al. Patient Selection for Long-Term Mechanical Circulatory Support: Is It Ever too Early for the NYHA Class III Patient?. Curr Hear Fail Opinion 2016