Cintilografia de perfusão miocárdica (CPM) é um exame de tomografia computadorizada por emissão de foto único (SPECT) que, através da infusão de um radiofármaco endovenoso e consequente emissão radiação ionizante (raios gama), fornece informações sobre perfusão, metabolismo e função ventricular.
O exame, de maneira mais completa utiliza duas fases, uma em repouso, onde o apenas injeta-se um rádiofármaco no doente e outra em stress onde, através de esforço físico ou estimulo farmacológico, consegue-se observar alterações da circulação coronariana através do aumento do fluxo sanguíneo miocárdico.
Ao solicitar ou interpretar este exame deve-se ter em mente 4 pontos-chave:
– qual a probabilidade pré-teste do meu paciente para patologia estudada ?
– qual razão da solicitação do teste: pesquisa de isquemia ? pesquisa de viabilidade ? pesquisa de inflamação do miocárdio ?
– se há ou não necessidade da fase de stress – bem como a escolha de qual método utilizar
– qual radiofármaco deve ser utilizado
A partir delas você terá melhor capacidade de extrair a maior quantidade de informações possíveis do exame.
A interpretação das imagens visa basicamente avaliar:
– alterações de perfusão ao stress e sua localização
–
reversibilidade ao repouso
RADIOFÁRMACOS DISPONÍVEIS
–
Tálio-201 ( TI-201): entra no miócito através da bomba de Na/K ATPase e seu clearance da célula depende da atividade da célula ( reduzida em células isquêmicas). Portando, se o estudo evidenciar, na fase de stress, hipocaptação em algum segmento do ventrículo e essa captação se normalizar durante a fase de repouso ( que para o Tálio deve ser feita ou 3-4 horas ou em 24 horas) estamos diante de uma isquemia transitória e com miocárdio viável.
– Tecnécio-99 (TC-99): Sestamibi ( nome do cátion lipofílico marcado com tecnécio mais utilizado): Entram passivamente no intracelular através de gradiente eletroquímico e se depositam nas mitocôndrias, comparado ao Tálio a redistribuição deste farmáco é mínima por isso são necessárias duas infusões do fármaco ( repouso e stress)
– Gálio (Gálio-67): confundido pelas células do corpo como semelhante ao ferro – é uma marcador de atividade e divisão celular, sendo portanto um marcador de atividade inflamatória. Comumente utilizado para pesquisa de miocardite ou na suspeita de rejeição em transplantados cardíacos.
Tálio x Tecnécio
Favorece Tálio:
1) Menor captação
esplênica e intestinal ( favorece interpretação da parede inferior)
2) A captação
do radiofármaco é maior em 1a passagem
3) Apresenta redistribuição
do radiofármaco ( necessita apenas uma injeção para stress e repouso)
Favorece Tecnécio:
1) Mais energia com melhor qualidade nas imagens (
maior determinante do uso do tecnécio preferencialmente )
2) Menor tempo de meia-vida permite o cálculo do
GATED / imagem mais precisa de captação de primeira passagem
TIPOS DE STRESS
Fisiológico
Através do aumento da frequência cardíaca ( por esteira ou bicicleta) eleva-se a frequência cardíaca e consequentemente a demanda metabólico dos miócitos, elevando-se assim o fluxo coronariano através dos mecanismos de regulação de fluxo coronariano e evidenciando isquemia em territórios com lesões coronarianas críticas
Contraindicações: incapacidade física de se exercitar, IAM < 4 dias, Estenose Aórtica Grave, Doença Arterial periférica grave, IC descompensada, Doença Valvar sintomática descompensada, PA > 220 x 110, Pericardite aguda, Dissecção de Aorta
Farmacológico (2 tipos):
1) Simpatomimético (Dobutamina): age através do aumento da contratilidade cardíaca e da frequência cardíaca estimulando receptores adrenérgicos – aumentando assim o consumo de oxigênio e aumento do fluxo sanguíneo para o miocárdio.
Contraindicações: IAM < 7 dias, Angina Instável, Estenose Aórtica grave, obstrução de via de saída do VE, arritmias atriais com resposta ventricular não controlada, história pessoal de TV, Dissecção de Aorta, HAS não controlada, uso de beta-bloqueador em que a resposta cronotrópico e inotrópica será atenuada.
2) Vasodilatadores ( adenosina, dipiridamol e ragadenoson):
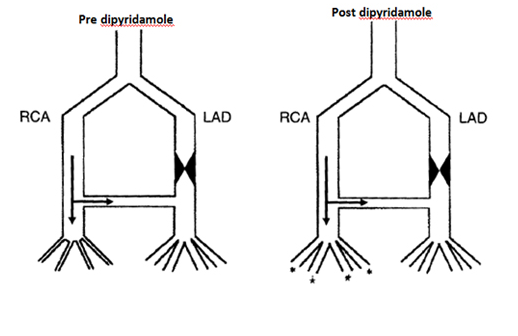
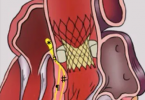
O uso de vasodilatadores baseia-se no princípio fisiológico de que os territórios coronarianos que já tem algum grau de obstrução (p.e. uma coronária com uma placa de >60% de obstrução luminal) já se encontram no ‘máximo’ de sua dilatação. Sendo assim, se eu realizar um estimulo vasodilatador coronário ( nesse caso através de fármacos ) as áreas com obstrução – já com dilatação máxima – não respondem e as áreas ‘normais’ ( sem obstrução coronária) respondem a esse estímulo aumentando seu calibre e ‘roubando’ para essa região o fluxo coronariano.Veja a ilustração:
 |
|
Figura 1: representativa de roubo de fluxo coronariano “horizontal”. A esquerda antes da infusão do vasodilator: note que o sistema arterial distal a lesão da LAD ( Artéria Descendente Anterior) encontra-se já vasodilatador ( sistema arteriolar – porção final da figura). A direita após infusão do vasodilator o sistema irrigado pela RCA ( Artéria Coronária Direita) também se vasodilatada e rouba fluxo do terriório da LAD – que por já estar previamente vasodilatado devido a lesão obstrutiva não consegue aumentar seu fluxo coronariano. Adaptado de Picano E. Stress Echocardiography 5th edition
|
Contraindicações: sibilância no momento do exame ( paciente asmáticos controlados podem fazer pré-tratamento com b2-agonista de curta duração – realizado em apenas alguns centros com retaguarda médica e de terapia intensiva), BAV 2o ou 3o graus, PAS < 90, uso de medicações contendo dipiridamol nas ultimas 48h, uso de metilxantinas nas ultimas 12 horas ( bloqueiam o efeito da adenosina) e hipersensibilidade prévia ao vasodilatador
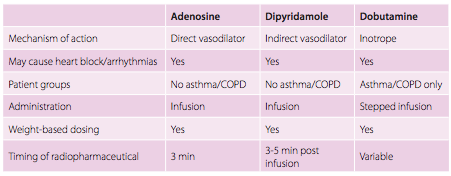 |
| Tabela 1: Resumo das principais drogas para stress farmacológico – fonte da EANM – Sociedade Européia de Medicina Nuclear e disponível aqui |
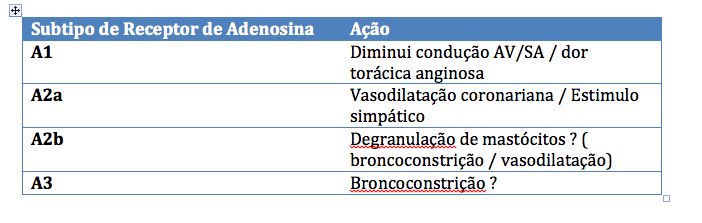 |
| Tabela 2: Subtipos de receptores de Adenosina e sua ação fisiológica. Fonte: aqui. |
Subtipos de receptores de Adenosina e sua ação fisiológica. Adaptado de http://www.dupharma.dk/?id=502&c=Adenosine-receptors-pharmacology-and-rapiscan.
RECOMENDAÇÕES PARA O STRESS
1) Preferir sempre que possível o stress fisiológico pois fornece outros dados prognósticos relevantes ( capacidade funcional, alterações eletrocardiográficas ao esforço, recuperação de frequência cardíaca).
2) O stress farmacológico apesar de aumentar a sensibilidade do exame (eleva o fluxo coronariano em 4-5 vezes o fluxo basal, enquanto o exercício fisíco eleva entre 2-2,5 vezes e meia, aumentando assim a capacidade de evidenciar heterogeneidade de perfusão coronariana) e, portanto, a presença de um exame alterado nem sempre implica que essa diferença de captação signifique que haja de fato isquemia (desbalanço entre demanda e oferta de oxigênio, pois ,como o estudo não é fisiológico, não há aumento da demanda de oxigênio pelos miócitos, podendo concluir num resultado falso positivo – Cuidado na interpretação de um teste positivo com stress farmacológico em paciente com probabilidade pré-teste baixa do exame.
3) Em caso de bloqueio de ramo esquerdo preferir uso de stress com vasodilator para se diminuir o efeito da elevação da frequência cardíaca na captação septal
4) O uso da dobutamina fica restrito a pacientes com contra-indicações ao exercício físico e a vasodilatadores
5) Suspender ou não o uso do beta-bloqueador ? O uso dos beta-bloqueadores / bloqueadores dos canais de cálcio e nitratos teoricamente diminuem a sensibilidade do exame e, em geral, sua suspensão é recomendada, principalmente em exames cujo stress é o exercício físico. No stress farmacológico, a literatura ainda é controversa e deve-se decidir individualmente ( exemplo: risco de arritmia ou descompensação de IC com suspensão do beta-bloqueador versus exame falso negativo). Uma situação em que toda a medicação do paciente deve ser mantida é a avaliação da eficácia do tratamento em um paciente com doença arterial coronariana já estabelecida.
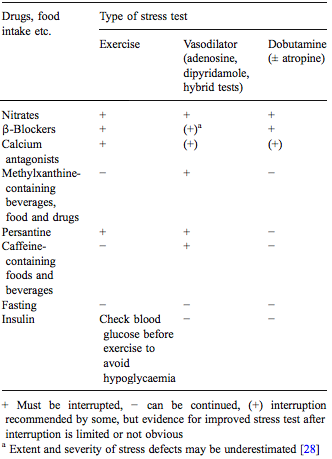 |
| Tabela 3: Recomendação da suspensão de drogas e medicações de acordo com o tipo de stress. Fonte European Journal of Nuclear Medicine and Molecular Imaging Vol. 32, No. 7, July 2005 disponível aqui |
CÁLCULO DA FRAÇÃO DE EJEÇÃO DO VENTRÍCULO ESQUERDO
Outra característica da cintilografia de perfusão miocárdica é o cálculo da fração de ejeção do ventrículo esquerdo através do método Gated – combina o eletrocardiograma do paciente com a aquição das imagens ventriculares permitindo ao examinador determinar o momento diastólico e sistólicos finais para o cálculo da FEVE. Vale ressaltar que a batida é criada através de uma média de aproximadamente 100 batidas com intervalo RR regular, garantindo a precisão do cálculo. Os valores de normalidade são acima de 50% para mulheres e 45% para homens.
Comparativamente ao ecocardiograma é uma medida menos operador-dependente e com menos variabilidade interobservador. Importante ressaltar também que os valores de FEVE encontrados num ecocardiograma não são comparáveis ao da cintilografia ( p.e um paciente masculino com FEVE de 55% no ECO e 45% no Gated – isto não implica em perda de função ventricular)
INTERPRETAÇÃO DOS RESULTADOS
Teste de stress:
 |
| Tabela 4 |
Teste de viabilidade:
 |
| Tabela 5
|
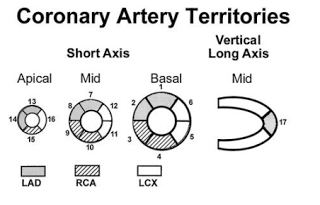
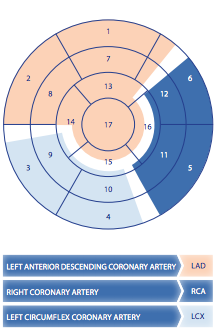
CORRELAÇÃO ENTRE TERRITÓRIO CORONARIANO E SEGMENTO ALTERADO
 |
|
Os 17 segmentos do VE com os respectivos territórios vasculares – retirado do guideline da
sociedade européia de medicina nuclear e disponível aqui
VIABILIDADE x ISQUEMIA: ENTENDO OS CONCEITOS
Conforme descrito na tabela 5, logo acima, o termo isquemia é utilizado para determinar uma hipocaptação do radiofármaco
em algum segmento miocárdico, sendo considerada ‘ transitória’ se é somente
ao stress ou ‘fixa’ se evidente tanto ao repouso quanto ao stress. A
grande questão está nesse tecido com ‘isquemia fixa’, na tabela identificada
como ‘infarto prévio’. Na maioria das vezes, de fato, esse tecido pode estar
morto e representar área de fibrose. Contudo, em algumas situações, o miocárdio
sofre de uma isquemia crônica que não leva a ‘morte celular/geração de fibrose’, mas
também não permite que o tecido tenha um metabolismo normal. Nesse caso, a
célula diminuiu o seu metabolismo ao mínimo possível para ainda preservar sua
vitalidade a espera de que, um dia, a circulação retorne a essa região e ela
possa voltar a funcionar normalmente.
Essa área é chamada de miocárdio
hibernante e suas células são viáveis, desde que voltem a receber nutrientes. A
detecção desse tecido é importante, por exemplo, se estamos em dúvida se uma
possível revascularização de coronária naquele território irá servir para
retornar a função de contratilidade miocárdica ou não.
Para tirarmos essa
dúvida, necessitamos utilizar técnicas diferentes da utilizadas para pesquisa
de isquemia, com o intuito de aumentar a sensibilidade do exame para detecção
de miocárdio viável. Uma opção é a utilização do tálio em uma fase de repouso (4h após stress) e
depois em uma segunda comparação em 24 horas. No primeiro momento, algumas
horas após a administração desse fármaco, as células ‘hibernantes’, por seu
metabolismo reduzido, podem não conseguir captar esse fármaco e, ao exame,
aparecerá uma área hipocaptante. Contudo, em um segundo momento, quando
observamos a imagem poderemos ver captação nesse local, denotando que o tecido
esta vivo, mas está lento! Caso não haja captação na fase tardia podemos
inferir, de fato, que o tecido não tem viabilidade.
Outra opção é o exame com
tecnécio em dois dias, no primeiro realiza-se a fase de stress e no segundo dia
com reinjeção do fármaco avalia-se o repouso. Outro técnica muito utilizada é a
administração de nitrato sublingual na fase de repouso com o intuito de
aumentar a sensibilidade do exame para detecção de miocárdio viável ( por
aumentar a perfusão em repouso). Por isso ao se deparar com uma cintilografia
miocárdica preste atenção no protocolo utilizado e se há necessidade de algum outro tipo de aquisição de imagem para pesquisa de viabilidade (p.e dispensada em caso de perfusão ao stress sem
alteração), como dito anteriormente a captação tardia implica em miócito vivo pois
o miócito necessita estar funcionante para o Tálio ( bomba Na/K) e com as
membranas celulares e mitocondrais intactas e gradiente eletroquímico
preservado para o tecnécio.
“PEGADINHAS”
1) Alterações de captação por artefatos:
– Mamas: hipocaptação fixa anterior, ântero-septal ou anterolateral
– Atenuação diafragmática: hipocaptação fixa inferior
– Tecido adiposo excessivo no tórax ( não das mamas): hipocaptação fixa lateral
– Movimento assincrônico do septo ( geralmente por BRE ou MP): hipocaptação fixa septal ( que pode piorar com o stress )
2) Cuidados com Indicações:
– Não pedir stress em SCA/dor torácica em paciente com dor recente (< 24-72h) ou na vigência de dor
Indicações clássicas do exame:
1) Investigação de equivalente isquêmico ( dispnéia, síncope, dor irradiada)
2) Investigação de angina estável
3) Investigação de dor torácica no pronto-socorro ( não fazer a fase stress se dor recente ou vigente no momento do atendimento )
4) Possível SCA de baixo/médio risco ( MNM negativos / ECG não isquêmico / score de risco de SCA baixo – exemplo: TIMI)
5) Investigação de DAC em pacientes de muito alto risco CV
6) Avaliação de significado funcional de lesão documentada por angiografia
7) Estratificação de risco CV antes de cirurgias não-cardíacas de médio ou alto risco em pacientes com 2 ou mais fatores de risco de Lee ( IRC com Creatinina > 2,0, IC, Doença isquêmica cardíaca, DM, AVE ou AIT)
8) Investigação de dor torácica crônica de média ou alta probabilidade
9) Após RM: após 5 anos ou após RM incompleta
10) Avaliação de viabilidade
11) Avaliação de função ventricular
Leitura sugerida
I Diretriz da Sociedade Brasileira de Cardiologia Sobre Cardiologia Nuclear 2002. Disponível aqui
2013 ESC guidelines on the management of stable coronary artery disease. Disponível aqui
Pitfalls and Limitations of Radionuclide and Hybrid Cardiac Imaging. Travin, MI. Disponível aqui
Radiotraçadores – Sociedade Brasileira de Cardiologia. Disponível aqui
Artifacts and Pitfalls in Myocardial Perfusion Imaging J Nucl Med Technol 2006; 34:193–211
EANM/ESC procedural guidelines for myocardial perfusion imaging in nuclear cardiology. Disponível aqui
Guidelines da Sociedade Americana de Medicina Nuclear. Disponível aqui e também aqui
Withholding or continuing beta-blocker treatment before dipyridamole myocardial perfusion imaging for the diagnosis of coronary artery disease? A randomized clinical trial. Disponível
|












Parabens a Caio Daniel Felipe e Jaime…. Blog sensacional…
Grande abraco deste leitor assiduo Anselmo Dantas